Wird die Johnson & Johnson FDA-Zulassung ICOTYDE zum Startschuss für eine neue Milliardenplattform im Immunologie-Geschäft?

Was bedeutet die Zulassung für Johnson & Johnson?
Johnson & Johnson meldet, dass die FDA ICOTYDE als interleukin‑23 (IL‑23) Rezeptorantagonist für erwachsene und jugendliche Patienten ab 12 Jahren und mindestens 40 kg Gewicht genehmigt hat, sofern diese für systemische Therapie oder Phototherapie infrage kommen. ICOTYDE ist damit die erste und bislang einzige gezielte orale Peptidtherapie, die den IL‑23‑Rezeptor direkt blockiert – ein zentraler Treiber der Entzündung bei Plaque-Psoriasis.
In vier Phase‑3‑Studien mit rund 2.500 Patienten erfüllte ICOTYDE alle primären Endpunkte und zeigte eine aus Anlegersicht wichtige Kombination aus hoher Wirksamkeit und einem insgesamt günstigen Sicherheitsprofil. In den Kopf-an-Kopf-Studien erreichten etwa 70 % der Patienten eine klare oder fast klare Haut (IGA 0/1), während rund 55 % einen PASI‑90‑Response nach 16 Wochen erzielten. Die Rate unerwünschter Ereignisse lag nahe am Placebo, ohne neue Sicherheitssignale bis Woche 52.
Damit unterstreicht die Johnson & Johnson FDA-Zulassung ICOTYDE den Anspruch des Konzerns, im stark wachsenden Markt zielgerichteter Immuntherapien eine führende Rolle einzunehmen. Ergänzend zu injizierbaren Biologika erweitert ICOTYDE das Portfolio um eine komfortable Einmal-täglich-Pille.
Wie reagiert die Börse auf die ICOTYDE-News?
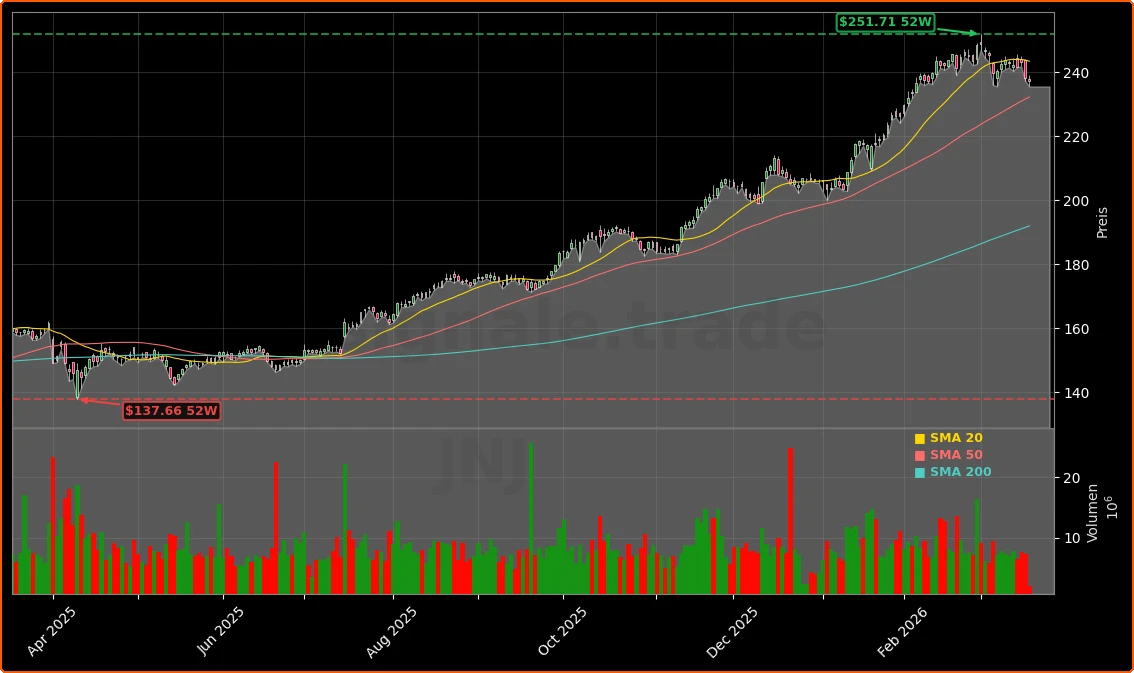
Die Aktie von Johnson & Johnson notiert aktuell bei rund 236,97 US‑Dollar und damit leicht unter dem Vortagesschluss von 238,70 US‑Dollar (‑0,48 %). Nach einem 52‑Wochen-Bereich von 141,50 bis 251,71 US‑Dollar bleibt der Kurs deutlich unter dem Hoch, bewegt sich aber klar im oberen Drittel der Spanne – von einem neuen Hoch kann also noch keine Rede sein.
Trotz kurzfristiger Gewinnmitnahmen bleibt die Stimmung der Analysten tendenziell positiv. HSBC hat ihr Kursziel laut jüngsten Einschätzungen auf 280 US‑Dollar angehoben und verweist neben der Onkologie-Pipeline auch auf die robuste Stellung des Konzerns im defensiven Gesundheitssektor. Citi‑Analysten sehen in ICOTYDE eine Therapie mit „Biologika‑Niveau bei der Wirksamkeit, kombiniert mit der Bequemlichkeit einer täglichen Tablette“, und modellieren potenzielle Spitzenumsätze von 5,5 Milliarden US‑Dollar für das neue Präparat.
Anleger sollten im Blick behalten, dass ICOTYDE zusätzlich in Studien zu psoriatischer Arthritis, Colitis ulcerosa und Morbus Crohn geprüft wird. Gelingt der Sprung in weitere Indikationen, könnte sich die Umsatzbasis deutlich verbreitern und die Johnson & Johnson FDA-Zulassung ICOTYDE zum Ausgangspunkt einer ganzen Wirkstoffplattform machen.
Warum ist ICOTYDE medizinisch ein Meilenstein?
Plaque-Psoriasis betrifft allein in den USA über acht Millionen Menschen und beeinträchtigt Lebensqualität, Arbeitsfähigkeit und psychische Gesundheit erheblich. Leitlinien empfehlen bei unzureichender Kontrolle mit topischen Therapien eine frühe Umstellung auf systemische Behandlungen. Genau hier setzt ICOTYDE an: Als gezielter IL‑23R‑Blocker greift der Wirkstoff in eine Schlüsselschnittstelle des immunologischen Entzündungskaskade ein und unterscheidet sich damit von breiter wirkenden Immunsuppressiva.
Patienten nehmen ICOTYDE einmal täglich morgens nüchtern mit Wasser ein und warten mindestens 30 Minuten bis zur Nahrungsaufnahme. Zu den häufigsten Nebenwirkungen zählen unter anderem Kopfweh, Übelkeit, Husten, Müdigkeit und Pilzinfektionen, während schwerwiegende Infektionen ein bekanntes Klasseneffekt-Risiko immunmodulierender Therapien darstellen. Für Anleger ist wichtig: Die bisherige Datenlage deutet auf ein Risiko-Nutzen-Profil hin, das eine breite ersteinsatzfähige Systemtherapie ermöglicht.
Strategisch positioniert sich Johnson & Johnson damit gegenüber Wettbewerbern wie AbbVie oder Eli Lilly im Kampf um Marktanteile im Milliardenmarkt für Psoriasis. Die orale Darreichungsform könnte insbesondere Patienten ansprechen, die Injektionen scheuen und bisher bei topischen Therapien verblieben sind.
Welche Bedeutung hat die Johnson & Johnson FDA-Zulassung ICOTYDE für Anleger?
Die Johnson & Johnson FDA-Zulassung ICOTYDE fällt in eine Phase, in der der Konzern sein Immunologie-Portfolio nach erwarteten Umsatzrückgängen bei älteren Blockbustern neu ausrichtet. Für Investoren eröffnet sich damit eine zusätzliche Wachstumsstory neben Onkologie und Medizintechnik. Institutionelle Investoren haben ihre Positionen zuletzt teils ausgebaut; so meldeten mehrere Adressen steigende Engagements, während das durchschnittliche Analystenkursziel laut verschiedenen Häusern weiterhin über dem aktuellen Kurs liegt.
„ICOTYDE ist ein potenzieller Game-Changer für viele erwachsene und jugendliche Patienten mit moderater bis schwerer Plaque-Psoriasis.“— Linda Stein Gold, Direktorin für dermatologische klinische Forschung, Henry Ford Health
Mit Blick auf die 52‑Wochen-Spanne bleibt die Bewertung zwar anspruchsvoll, doch starke Cashflows, Dividendenhistorie und ein breites Pipeline-Portfolio machen die Aktie für langfristig orientierte Anleger interessant. Kurzfristig dürfte der Markt nun erste Verschreibungsdaten und mögliche weitere regulatorische Fortschritte bei ICOTYDE in zusätzlichen Indikationen genau verfolgen.
